近日,芝加哥大学化学系John T. Wilson杰出讲席教授何川荣获2023年度四面体创新奖(Tetrahedron Prize),以表彰他在有机化学以及生物有机与医药化学领域的杰出贡献。四面体创新奖由《四面体》系列杂志设立,是有机化学、化学生物学与药物化学领域的重要国际奖项。ACS Chem. Biol. 杂志特发表In Focus文章“Opening New Avenues in Bioorganic Chemistry: Prof. Chuan He Receives the Tetrahedron Prize”,介绍何川教授的工作及其对科学界的影响,文章作者为伊利诺伊大学香槟分校的赵伯譞助理教授和北京大学陈鹏教授。
何川教授的研究范围广泛,涉及化学生物学、核酸化学与生物学、表观遗传学、生物化学、分子生物学和基因组学。近年来,他主要关注生物体中可逆的RNA和DNA甲基化修饰问题,他的实验室于2011年发现了可逆RNA甲基化调控基因表达的新机制,还通过发展新的工具技术率先研究了哺乳动物基因组中5-羟甲基胞嘧啶(5hmC)的生物学相关机制。作为世界上最负盛名的有机化学奖项之一,此次的四面体创新奖表彰了何川教授在多学科领域交叉研究尤其可逆核酸修饰的调控方向的突出贡献,同时也验证了现代有机化学的演变及其与生物学研究的深刻联系。何川教授目前还担任ACS Chem. Biol.杂志的主编,在此之前,该杂志的创始主编Laura L. Kiessling教授也曾于2017年获得四面体创新奖。

回顾何川教授的科研历程,我们不难发现,这是一个不断开拓与创新的故事。何川教授1972年出生于中国贵州省,1994年于中国科学技术大学获得应用化学学士学位。之后,他在生物无机化学领域的先驱和创始人,麻省理工学院Stephen J. Lippard教授指导下于2000年获得化学博士学位。在研究生期间,他的主要研究方向是仿生物的化学研究,通过有机合成开发了多种新型金属配体,共计发表九篇论文。此后,他获得Damon Runyon博士后奖学金,前往哈佛大学Gregory L. Verdine教授课题组开展博士后研究。在Verdine实验室,他接受了核酸相关生物有机化学的训练,在DNA修复领域,特别是大肠杆菌DNA修复蛋白N-Ada及其对甲基磷酸三酯损伤的修复方面做出了有意义的研究成果。这些早期阶段的工作开启了何川教授的职业生涯,并使其关注化学与生命科学学领域交叉研究的重要问题。

何川教授于2002年在芝加哥大学开始了独立的科研生涯,在有机合成方法学和新型金属催化剂的开发,特别是金催化的有机转化方面进行了研究。同时,他继续在生物无机化学,特别是研究和设计大量金属离子识别蛋白和DNA修复蛋白领域进行了深入探索。他的研究后来也扩展到微生物领域,探究人类病原体的抗生素耐药和毒力调节机制,并成功鉴定了金黄色葡萄球菌和铜绿假单胞菌的关键调节因子。尽管这些早期研究都获得了成功,何川教授仍然在2008年决定进行调整,追求和挑战一个全新的科学方向,即生物大分子动态化学修饰类型和功能的多样性,同时试图回答重要的科学问题,即早期胚胎细胞是如何从一个相同的基因组发展出丰富多样的类型。结合实验室在有机化学,核酸生物化学和化学生物学方面的优势,何川教授的大胆选择最终使他成功开创了表观转录组学即RNA表观遗传学领域,并在科学界留下了浓墨重彩的一笔。
由于在DNA修复领域具有丰富的研究经验,何川教授首先专注于破译DNA上的化学修饰。他发表的一系列开创性的工作,特别是DNA甲基化的可逆修饰研究,对癌症研究及其他领域都产生了深远的影响。此外,实验室也开发了一系列基于酶和化学工具的测序技术,以解析5-甲基胞嘧啶(5mC)的氧化中间体的精确位置,帮助理解了TET酶如何通过催化 5mC的逐步氧化最终产生未修饰的胞嘧啶,从而实现DNA去甲基化的复杂过程。这些研究不仅揭示了 DNA修饰的动态和可逆性,为开发疾病(如癌症)新疗法奠定基础,同时也启发了何川教授在RNA的可逆化学修饰领域的工作,下面我们将对其进行介绍。
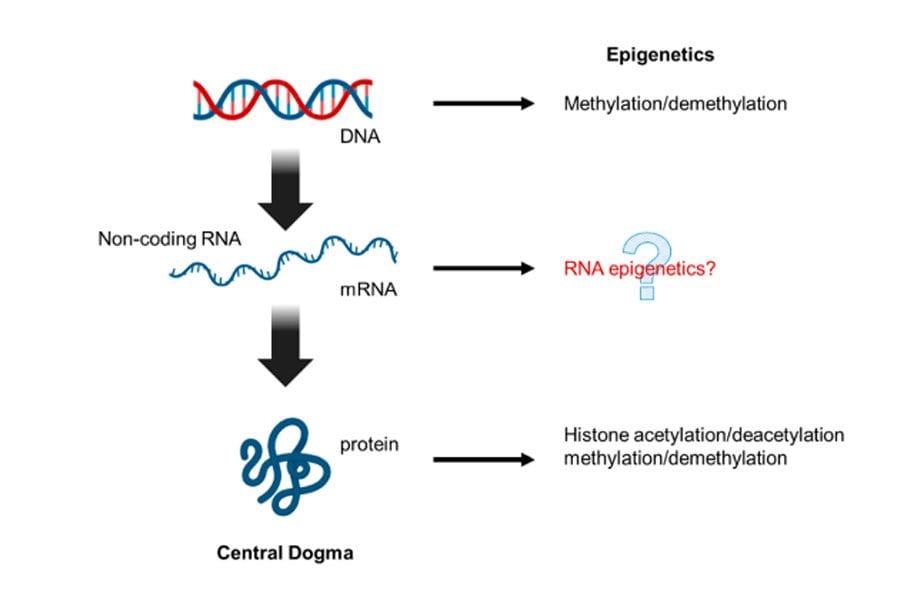
RNA拥有170种以上独特的化学修饰,这其中N6-甲基腺苷(m6A)是真核生物中最普遍的mRNA修饰。引人注目的是,尽管它的发现早至20世纪70年代,但直至何川教授的开创性研究问世以前,m6A的生物学功能和意义在很大程度上仍迷雾重重。基于实验室对于AlkB家族蛋白去甲基化活性和生物有机化学方面的专业知识,何川教授迅速聚焦到与AlkB同源的肥胖相关蛋白-FTO上,并合成了一组带有化学修饰的核苷底物来测试酶活。他们的第一项体外研究发表于2008年,报道了FTO对单链RNA分子的去甲基化催化活性,随后在2011年,他们又首次报道了FTO胞内催化RNA的m6A修饰去甲基化活性。这项工作验证了何川教授在2010年提出的推论,即存在一种基于可逆RNA甲基化修饰的新的基因调控模式。此外,何川教授于同年还预测了“阅读器”蛋白的存在,其通过结合特异性RNA修饰以实现生物功能,并强调了对这些修饰的位置进行测序的重要性。在这些突破性的工作之后,何川实验室迅速发表了许多重要的研究以建立完整的m6A调控机制概貌,包括第二个去甲基化酶ALKBH5的鉴定,m6A甲基化酶复合体的核心亚基METLL3和METTL14以及辅助因子如WTAP的组成表征,以及作为m6A直接结合底物从而影响mRNA生命周期等性质的YTH家族蛋白的鉴定和功能研究。在短短的五年时间里,这一系列研究成果奠定了RNA表观遗传学即表观转录组学领域的基础,到目前为止,有7000多篇已发表的研究论文描述了m6A在多种生命系统中的功能。RNA修饰现在被认为在基因调控中扮演着核心角色,这方面的研究对理解生命过程(包括发育、免疫反应和疾病进展等)具有深远的影响。
从何川教授杰出的职业生涯中,我们可以看到现代有机化学在过去几十年里经历了怎样的范式转变。这种转变将继续发展并进一步与现代生物医学相交叉融合,发展出多种研究领域,例如:
- 化学生物学: 有机化学家越来越多地与生命科学家合作,打破了化学和生物学之间的传统界限。这种跨学科的方法,被称为化学生物学,其致力于使用化学工具和原理来回答诸多复杂的生物学问题。何川教授的工作通过利用有机化学概念和方法来揭示生物学过程的新调控机制(如表观遗传学和表观转录组学),都很好地证明了这种整合科学的重要意义。
- 靶向药物发现和个体化精准医疗: 有机化学与生物学的结合加速了药物和靶向治疗的发展,这种整合可以通过大规模的小分子文库的制备,帮助发现具有新生物或治疗特性的药物分子,或与主要疾病相关靶点相互作用的小分子,使研究人员能够更好地了解疾病的分子基础,并通过化学遗传学设计精确的干预措施。此外,通过了解个体独特的遗传和表观遗传特征,可以设计量身定制的疗法,以最大限度地提高治疗效果和减少副作用。
- 化学合成的创新: 有机化学和生物学之间的协同作用也激发了化学合成技术的持续创新。从天然产物的仿生合成到生物催化剂的发展,研究人员正在开发新的化学反应和方法,能够精确地创造复杂的分子。有机化学的创新进而推动了催化、合成、分析技术和自动化方面的研究进步,对药物发现和材料科学等领域做出了重大贡献。
何川教授从一个对科学充满好奇的青年成长为享誉全球的科学家,他的学术历程体现了对科学探索不懈努力和追求卓越的过程。他在表观遗传学和表观转录组学方面的开创性工作,彻底改变了我们对RNA化学修饰的理解,为基础生物学和疾病治疗提供了新的可能性,也为他赢得了多项著名奖项,包括沃尔夫奖,保罗·马克斯奖,Falling Walls生命科学突破奖,以及本次的四面体奖。这些奖项是对何川教授科学创新贡献的肯定,也凸显了有机化学在推进生物学研究、药物发现以及在分子水平上理解生命进程的关键作用。何川教授对于交叉领域的不懈探索也将激励新一代的年轻科学家对于前沿跨学科研究的孜孜追求。

Opening New Avenues in Bioorganic Chemistry: Prof. Chuan He Receives the Tetrahedron Prize
DOI: 10.1021/acschembio.3c00557